Antikörper, Antikörper, Antikörper! Ganz, ganz, ganz viele bitte? Hm. Habt ihr euch schon mal übergessen? - Schauen wir uns heute also die lymphoiden T-Zellen ein wenig näher an mit Fokus auf die CD8
https://viamedici.thieme.de/lernmodul/549574/539522/
Das wohl verrückteste und momentan völlig in orwellschem Neusprech verpackte Thema sind die T-Zellen. Da sie ein so unvorstellbar breites Repertoir im adaptiven (nicht angeborenen, spezifischen Immunsystem) ausmachen und das Maß aller Dinge, gerade bei viralen Infektionen darstellen. (Wobei man sagen muss, dass durch das Komplementärsystem die Frage im Raum steht, ob man die lymphozytischen Zellen wirklich nur dem adaptiven Immunsystem zuschreiben will?)
“Das Immunsystem besteht aus einer angeborenen (nicht-adaptiven, natürlichen, unspezifischen) und einer erworbenen (adaptiven oder spezifischen) Immunität, die den Körper vor Mikroorganismen (Viren, Bakterien, Parasiten und Pilze), „fremden“ Makromolekülen und entarteten Zellen schützen. Die Zellen des Immunsystems erkennen diese Fremdkörper anhand charakteristischer Proteinmuster, den Antigenen.”
Antigene… hm….. Quizfrage: Wie funktioniert das denn überhaupt? Und genau da wird es eben so unglaublich kompliziert, dass einem schwindelig wird:
(Grundverständnis, wie und wo die neutralen T- und B- Zellen zu finden wären.)
https://www.jimmunol.org/content/205/3/608
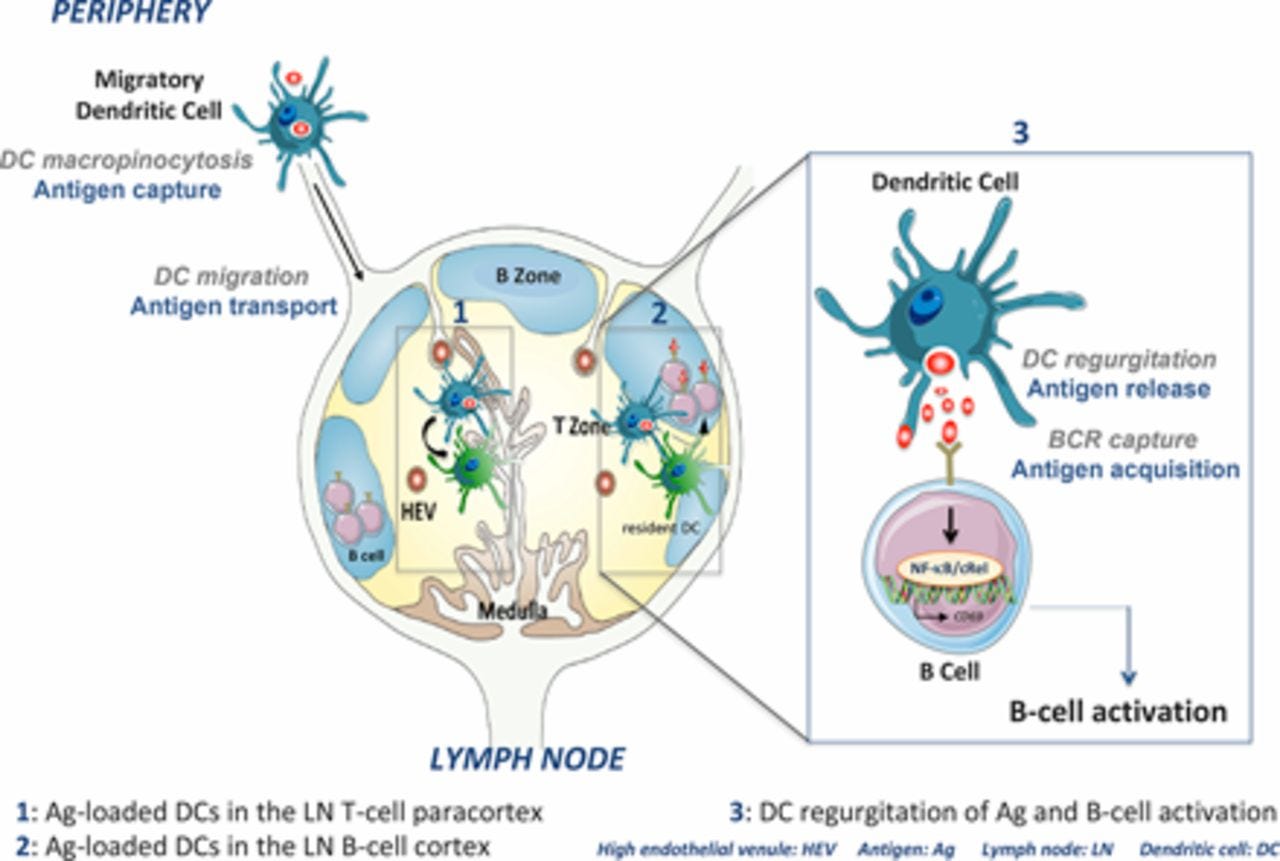
”Dendritische Zellen (DCs) sind professionelle APCs (antigenpräsentierende Zelle), die Ags (Antigene) in der Peripherie aufnehmen und zu den Lymphknoten wandern, wo sie T-Zellen aktivieren. DCs können durch in vitro und in vivo beobachtete Interaktionen auch native Ag auf B-Zellen übertragen. Die Mechanismen des Ag-Transfers und der B-Zell-Aktivierung durch DCs sind jedoch noch nicht vollständig geklärt. In dieser Studie berichten wir, dass DCs in der Maus ein wichtiger Zelltransporter von Ag aus der Peripherie in die B-Zell-Zone des Lymphknotens sind und sowohl in vivo als auch in vitro eine B-Zell-Aktivierung bewirken. Wichtig ist, dass wir einen neuen extrazellulären Mechanismus der B-Zell-Aktivierung durch DCs aufzeigen. In dieser Studie zeigen wir, dass Ag, das bei der Ausschüttung von DCs freigesetzt wird, ausreicht, um eine frühe B-Zell-Aktivierung zu bewirken, die durch den BCR (B-Zell-Rezeptor) gesteuert wird und mechanistisch von der nukleären Akkumulation des Transkriptionsfaktors NF-κB/cRel abhängt. Somit bietet unsere Studie neue mechanistische Einblicke in die Modalitäten der Ag-Freisetzung und B-Zell-Aktivierung durch DCs und einen vielversprechenden Ansatz für die gezielte Beeinflussung des NF-κB/cRel-Signalwegs zur Modulation der DC-ausgelösten B-Zell-Reaktionen.”
Aha. Also heißt das zwangsläufig, dass auch schon bei der Differenzierung von B - und T-Zell-Aktivierung der NF-kB-Signalweg eine Rolle spielt.
Kurze Randbemerkung, die als eine Frage stehen bleiben wird: Würde das auch für Natürliche Killerzellen (NK) gelten?
Gut, dass ich versuchte, die kritische Rolle von Signalwegen und deren absolute Doppelzüngigkeit schon in meinem letzten Substack ein wenig herauszuarbeiten:
Wir müssen reden
We have to talk (english)
”Was sind dendritische Zellen?
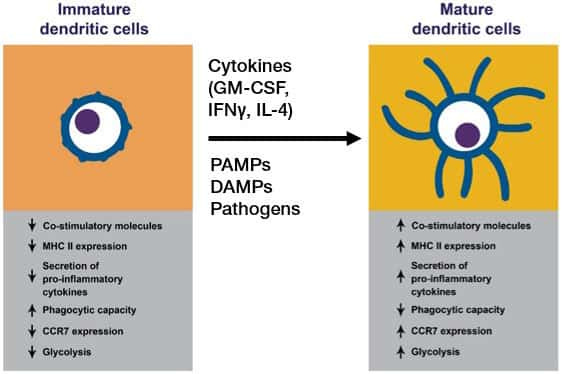
Dendritische Zellen (DCs) spielen eine zentrale Rolle bei der angeborenen Erkennung von Krankheitserregern und der anschließenden Aktivierung der adaptiven Immunantwort. DCs leiten die adaptive Reaktion ein, indem sie antigene Peptide auf Molekülen des Haupthistokompatibilitätskomplexes (MHC) präsentieren, um die Aktivierung und Differenzierung von T-Zellen zu bewirken. DCs sezernieren auch Zytokine und Wachstumsfaktoren, die die Immunreaktion verstärken und modulieren. Neben ihrer Rolle bei der Aktivierung naiver T-Zellen spielen DCs vermutlich auch eine entscheidende Rolle bei der Steuerung der Differenzierung regulatorischer T-Zellen sowie bei der Entwicklung von T-Zell-Toleranz. Als wichtige Sentinel-Zellen sind sie überall im Körper zu finden, insbesondere in den lymphatischen Organen und an Grenzflächen zur Umwelt wie dem Darm und der Haut.”
Es ist unglaublich schwer, wirklich zu verstehen, was da eigentlich passiert, da innerhalb der eukaryotischen Zellen sehr, sehr viele Prozesse zeitgleich ablaufen und besonders für die Aktivierung und Differenzierung der Immunantwort endlos viele Faktoren reinspielen. So auch die Umgebung, wo sie gebildet werden und noch andere Zellen, sowie die Cytokine:
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3312336/
”Während des Differenzierungsprozesses spielen die Migration von Thymozyten durch diskrete thymische Mikroumgebungen und der Kontakt mit dem Peptid-MHC-Komplex (pMHC) auf verschiedenen thymischen Antigen-präsentierenden Zellen (APCs), einschließlich der kortikalen thymischen Epithelzellen (cTECs), medulläre Thymusepithelzellen (mTECs) und dendritische Zellen (DCs) eine entscheidende Rolle bei der Gestaltung des T-Zell-Repertoires für die Antigenerkennung, den Selektionsprozess und die Expression von Oberflächenmolekülen von CD4 und CD8.”
Ich versuche es dennoch einmal möglichst “simpel” mit vielen Bildern unterstrichen:
doi: 10.1038/nri.2015.10
Es wird prinzipiell in 2 Arten von T-Zellen unterschieden: CD8 und CD4-T-Helfer-Zellen. CD8 sind zytotoxische T-Zellen. Neben diesen gibt es noch, wie schon oben erwähnt, die B - und NK-Zellen.
Und hier wird es richtig tricky
Ich fasse es erst einmal kurz wirklich grob zusammen: Die neutralen T-Zellen (sowohl CD4 als auch CD8) docken durch spezifische Rezeptoren an die dendritischen Zellen an. Es wird ein Antigen präsentiert und aus den neutralen werden aktivierte T-Zellen. Die CD4 hat einen MHC-Klasse II-proteinspezifischen Rezeptor. Die CD8 MHC-Klasse I.
https://rupress.org/jem/article/196/8/1013/39527/Antigen-Presentation-by-Dendritic-Cells-In-Vivo
Symboldbild aus einem Youtubevideo
Während die CD8+ das spezifische Antigen präsentiert bekommt, hat die aktivierte CD4+ unterschiedlichste Rollen: Von T-Helferzellen (TH1,2, 17, 9) über regulatorische T-Zellen (Treg), die für eine Balance sorgen bis hin zu regulatorischen T-Helferzellinien, welche die B-Zell-Aktivitäten orchestrieren, den sogenannten follikulären T-Helferzellen (Tfh)
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3312336/
“CD4+T-Zellen sind von entscheidender Bedeutung für eine regulierte, wirksame Immunantwort auf Krankheitserreger. Naive CD4+T-Zellen werden nach der Interaktion mit dem Antigen-MHC-Komplex aktiviert und differenzieren sich in spezifische Subtypen, die hauptsächlich vom Zytokinmilieu der Mikroumgebung abhängen.”
Ich muss offengestehen, dass mir für die CD4-T-Zellen momentan noch sehr viel Basisverständnis fehlt, um genauer erklären zu können, unter welchen Regeln diese ungalublich komplexe Differenzierung in T-Helferzellen der einzelnen Klassen, Treg und Tfh statt findet.
Und mein Hauptaugenmerk mag ich in diesem Artikel auf die CD8 richten.
Ich versuche es möglichst einfach zu halten und werde mich dabei durch folgenden Artikel hangeln, der mir sehr weiter half, es zu verstehen.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5900024/
Beginnen wir mit dem Abstrakt, was schon sehr aufschlussreich war:
”Der Mensch ist sehr anfällig für Infektionen mit Atemwegsviren wie dem Respiratory Syncytial Virus (RSV), dem Influenza-Virus, dem Humanen Metapneumovirus, dem Rhinovirus, dem Coronavirus und dem Parainfluenza-Virus. Während einige Viren lediglich die Symptome einer Erkältung hervorrufen, führen viele Atemwegsviren nach einer Infektion zu schwerer Bronchiolitis, Lungenentzündung und sogar zum Tod. Trotz der immensen klinischen Belastung gibt es für die meisten der am häufigsten vorkommenden Lungenviren keine lang anhaltenden, wirksamen Impfstoffe. Fast alle derzeitigen Impfstrategien zielen darauf ab, breit neutralisierende Antikörper zu erzeugen, die nach einer nachfolgenden Infektion eine schwere Erkrankung verhindern. Die mukosale Antikörperreaktion auf viele Atemwegsviren ist jedoch nicht von langer Dauer und nimmt mit zunehmendem Alter ab. CD8-T-Zellen sind entscheidend für die Beseitigung vieler akuter Virusinfektionen in der Lunge. Darüber hinaus sind CD8-T-Gedächtniszellen in der Lage, einen Schutz vor Sekundärinfektionen zu bieten. Daher kann die kombinierte Induktion von virusspezifischen CD8-T-Zellen und Antikörpern eine optimale Schutzimmunität bieten. Wir geben einen Überblick über die aktuelle Literatur zu CD8-T-Zell-Reaktionen, die durch Infektionen mit Atemwegsviren ausgelöst werden. Darüber hinaus wird untersucht, wie dieses Wissen bei der Entwicklung künftiger Impfstoffe gegen Atemwegsviren genutzt werden könnte, wobei der Schwerpunkt auf der RSV-Impfung liegt.”
Den Schwurbel über die Impfungen kann man getrost ignorieren: Es gibt keinen Impfstoff, der jemals wirklich erfolgreich gegen Influenza oder Coronaviridae entwickelt wurde.
https://www.abc.net.au/news/health/2020-04-17/coronavirus-vaccine-ian-frazer/12146616
https://www.nbcnews.com/health/health-news/flu-shot-fail-why-doesn-t-vaccine-always-work-n21446
Dazu muss man sich nur folgende Frage stellen: Welche Eigenschaften haben COVs und Influenzaviren gemein?: Sie mutieren und das zuverlässig und schnell. Wenn ein Antigen von letztem Jahr präsentiert wird, darfst du dir sicher sein, dass das neue Influenzavirus darauf nicht mehr anspringen wird und bestenfalls noch einen Teil des Epitopsets vom letzten Jahr beinhaltet.
https://www.nature.com/articles/ni.3056
Es funktioniert einfach nicht. Der beste Schutz ist und bleibt eine frühe Behandlung der Symptomatik + Stärkung des zellulären Arms durch Vitamin D, K2, Zink, etc… (Bitte nicht als medizinische Anleitung verstehen).
Zurück zu der Studie:
“Nach einer akuten Atemwegsinfektion stimulieren dendritische Zellen (DCs), die virales Antigen aufgenommen haben, die Aktivierung naiver CD8-T-Zellen in den drainierenden Lymphknoten der Lunge, um eine robuste virusspezifische CD8-T-Zell-Antwort auszulösen. Die Infektion mit Atemwegsviren in Mausmodellen führt zu einem Anstieg der Häufigkeit und Anzahl der gesamten und antigenspezifischen CD8-T-Zellen in der Lunge und den Atemwegen.”
Habt ihr aufgepasst, wo die dendritischen Zellen zu finden sind und wo sie das Antigen präsentieren, wenn sie gereift sind? Wieso war von Anfang an klar, dass ohne eine IgA-Antwort auf den Schleimhäuten faktisch die gesamte Transfektionsschussnummer höllisch nach Hinten losgehen wird? (Dazu gleich noch mehr.)
Insgesamt könnte man die gröbste und wichtigste Funktion der CD8- und CD4-Funktion wie folgt zusammenfassen: Während das CD4 das Zusammenspiel von Antikörpern, regulatorischen Helferzellen und T-Helferzellen orchestriert, indem es sich in diese ausdifferenziert, bilden die dendritischen Zellen antigenspezifische CD8+, die sich - wie durch ein Wunder - in den ersten Tagen der Infektion vermehren und das Virus bekämpfen. Anschließend werden gut 90 - 95 Prozent wieder abgebaut, weil sie nicht mehr gebraucht werden, während aus den TH1 und TH2 (CD4-Helferzellen) Gedächtnis-T-Zellen gebildet werden. - Was genau sie mit den freigesetzten Zytokinen machen, ist einfach zu komplex und mega-kompliziert, als dass ich an dieser Stelle weiter ins Detail gehen könnte.
Ich denke, wer sich diese wunderschöne, und wirklich gut zu verstehende Studie weiter durchliest, wird mir jetzt auf meinem Ausflug in die Welt der dummen Ideen, den ich hier noch kurz machen werde, zum Thema T-Zell-Harmonie und nutzlose Antikörper, ohne Probleme folgen können:
Bitte an dieser Stelle nun nicht wundern. Ich muss kurz zu den B-Zellen und den nutzlosen Antikörpern springen, was jedoch beim Weiterlesen Sinn machen wird, wenn ihr im Hinterkopf behaltet, dass die CD4 zeitgleich mit den CD8 aktiviert werden und ERST DANN im Blut die B-Zellen als Helfer mit Antikörpern.
Was schrieb da das öffentliche Gesundheitsportal für Österreich noch mal (sprich vom österreichischem Gesundheitsministerium) zu IgA - und IgG - Antikörpern?: Ach ja:
“Antikörper vom Typ IgA
Antikörper vom Typ Immunglobulin-G (IgA) sind vor allem in Körpersekreten wie Speichel, Tränenflüssigkeit, Magensaft, anderen Verdauungssäften, Nasenschleim, Lungensekret, Muttermilch etc. enthalten. Sie erfüllen die folgenden Funktionen:
Bindung von Mikroorganismen auf Schleimhäuten und Aktivierung von Entzündungsreaktionen;
der hohe Anteil von IgA in der Muttermilch ist ein wichtiger Schutzfaktor gegen Brech- bzw. Durchfallserkrankungen des Säuglings.”
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8897957/
Und hier ein kleiner Witz für Pfeyzer und die anderen Transfektions und GEN-Therapeutika:
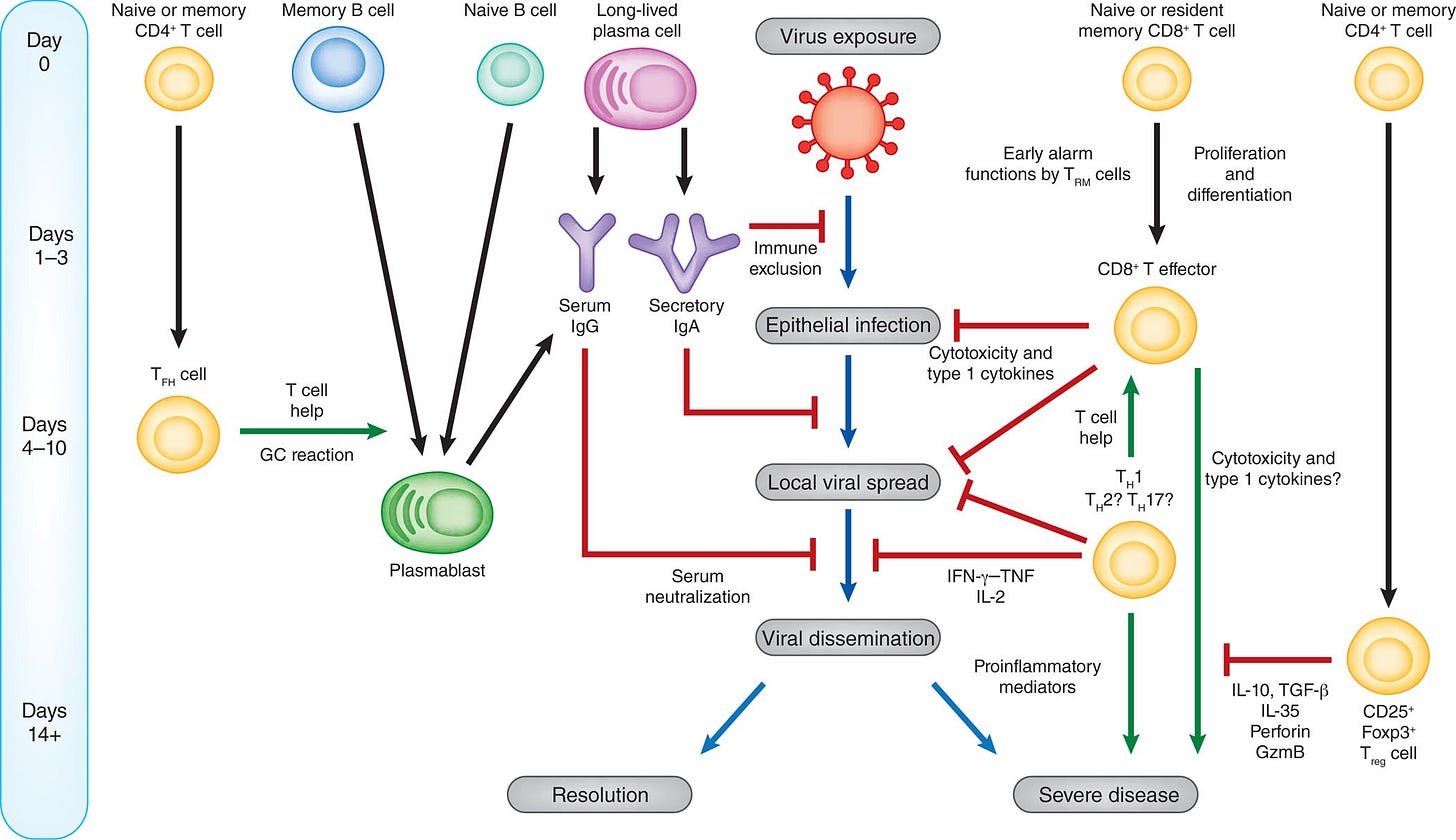
https://www.nature.com/articles/ni.3056/figures/1
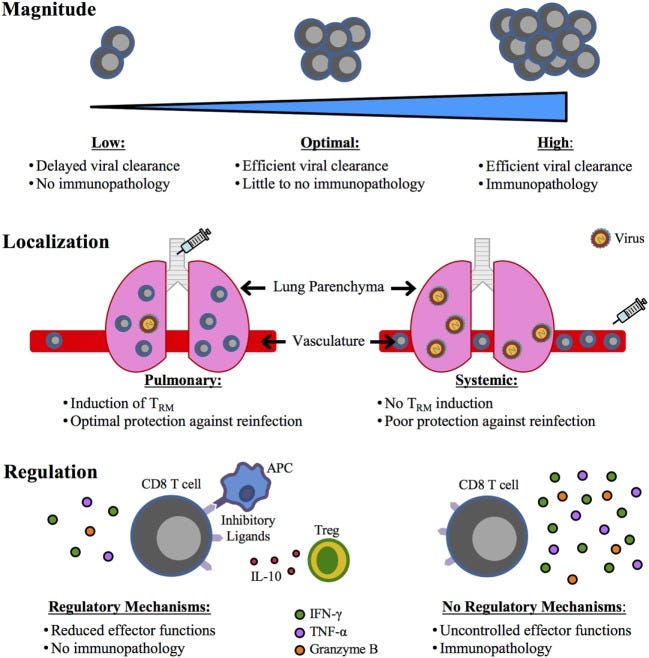
”Während einer akuten Virusinfektion der Atemwege wirken die humorale und die zellvermittelte Immunität zu unterschiedlichen Zeitpunkten, um die Krankheit zu begrenzen. IgA in der Schleimhaut, das bei einem früheren Kontakt mit dem Virus gebildet wurde, kann die Infektion verhindern oder begrenzen. IgG in der Lunge kann eine schwerere Erkrankung begrenzen. T-Zellen sind bei der Eliminierung virusinfizierter Zellen von Vorteil; sie koordinieren eine regulierte Immunantwort und fördern als TFH-Zellen hochaffine, dauerhafte Antikörper. Gelingt es nicht, die Virusausbreitung zu kontrollieren, kann dies zu einer schweren Erkrankung führen. Treg-Zellen hemmen die Effektorantworten durch verschiedene Mechanismen, darunter suppressive Zytokine (IL-10, IL-35 und TGF-β) und möglicherweise die aktive Abtötung durch Perforin und Granzyme B (GzmB). Eine überschießende oder schlecht regulierte Immunantwort kann auch zu schädlichen Immunpathologien führen.”
Und weiter heißt es:
”Außerdem rekrutieren Entzündungsmediatoren angeborene Zellen, darunter Neutrophile und vor allem natürliche Killerzellen. Diese sind in der Lage, virusinfizierte Zellen über von Perforin-Granzymen abhängige Mechanismen und das Typ-II-Transmembranprotein-Zytokin FasL über seinen Rezeptor Fas (CD95) abzutöten, sowie die Produktion von Interferon-γ (IFN-γ) mit seinen verschiedenen immunstimulierenden Wirkungen und der Polarisierung ankommender T-Zellen zu einer eher antiviralen, zytolytischen T-Helfer-Typ-1-Antwort (TH1).”
(Ihr erinnert euch: CD4-Differenzierung)
Zurück nach Österreich:
”IgG, IgA und IgM.
Eine insgesamte Vermehrung der Antikörper im Blut wird Hypergammaglobulinämie genannt. Dabei ist die Unterscheidung der folgenden zwei Formen erheblich:
polyklonale Gammopathie: Vermehrung vieler verschiedener Immunglobuline im Blut. Oft liegt hier ein reaktives Geschehen (d.h. der Körper reagiert auf etwas) zugrunde – z.B. chronische Entzündungsprozesse. Darüber hinaus kann auch eine Autoimmun- oder schwere Lebererkrankung (z.B. Leberzirrhose) vorliegen.
monoklonale Gammopathie: Vermehrung eines bestimmten Immunglobulins vom selben Typ im Blut. Das kann einen Hinweis auf eine bösartige Erkrankung (ein malignes Lymphom) darstellen. Es kann sich aber auch um eine bedeutungslose Erscheinung unbekannter Ursache handeln.”
Für die unter euch, die sich noch tiefer in die IgM, IgA, IgG-Geschichte einlesen wollen (danke, Maples.)
https://www.jimmunol.org/content/194/1/13
“Das kann einen Hinweis auf eine bösartige Erkrankung (ein malignes Lymphom) darstellen.” - Warum haben wir immer wieder betont, dass monochlonale Antikörper ausgerechnet gegen die Spike-Epitope inklusive dem GAG, GP41 und 120 - HIV1-Virus-Epitopen eine unvorstellbar schlechte Idee sind? Zu diesem Thema bitte ich euch, euch in Ruhe meinen 3. Artikel über die zerschossenen T- und B-Zellen durchzulesen.
Englisch:
Über negative Effektivität und zerschossene B- und T-Zellen.
Deutsch:
Über negative Effektivität und zerschossene B-und T-Zellen.
Ihr erinnert euch an den Anfang diesen Artikels, als ich herausgearbeitet habe, dass auch das WO eine Rolle spielt? → LNPs in den Ovarien? LNPs wo? Leber, Niere, Milz, Herz?
https://www.tga.gov.au/sites/default/files/foi-2389-06.pdf
Schließen werde ich mit einem weiteren Fallbeispiel, dass mit diesen Zellen russisch Roulette mit 7 Patronen in der Revolverkammer gespielt wurde und damit, was bei einer Depletion der neutralen T-Zellen so schief gehen kann.
https://www.frontiersin.org/articles/10.3389/fimmu.2021.741218/full
Ich wollte euch an dieser Stelle dann doch die Qual ersparen, anzumerken, dass sich die T-Zellen auch noch in 2 Subklassen unterteilen: Und zwar in klassische αβ-T-Zellen (Alpha-Beta) und kaum verstandenen und weniger häufig vorkommende γδ-T-Zellen (Delta-Gamma). - Auch wenn ich es heute Morgen ankündigte. Mir sind zu viele Ungereimtheiten in der Studie, die ich eigentlich noch besprechen wollte, aufgefallen. - Wer sich einlesen mag, das Paper ist recht gut geschrieben.
Zeigen wir also noch fix, warum die T-Zellen so essentiell sind:
https://www.frontiersin.org/articles/10.3389/fimmu.2021.684014/ful
“Unsere Daten zeigen eindeutig eine deutlich stärkere Induktion von SARS-CoV-2-spezifischen CD8+ T-Lymphozyten und eine höhere IFNγ-Produktion bei Patienten mit leichter im Vergleich zu Patienten mit schwerer oder kritischer COVID-19. Bei allen Patienten wurden SARS-CoV-2-spezifische Antikörper mit ähnlicher neutralisierender Aktivität nachgewiesen, die höchsten Titer an Gesamt-IgG wurden jedoch bei kritischen Patienten beobachtet. “
Wie war das gleich wieder mit der ausbleibenden nucleocapsid Antwort? Was schrieben die Engländer gleich wieder?:
Was so schief gehen kann, wenn die CD4 kaputt geht...
Ich denke, die Überschrift kann sich jeder selbst übersetzen oder ahnt zumindest, worauf das Ganze hinausläuft.
Vielen Dank auch hier, lieber Maples, für diese großartige Studie:
Bitte versteht diesen Punkt nicht falsch: Neutralisierende Antikörper, insbesondere IgA, sind die erste Bastion einer gesunden Immunantwort. Und sie helfen auch als bindende- und neutralisierende Antikörper orchestriert von den CD4 bei einer schweren Infektion. Aber genau da liegt die Krux: Bei einer SCHWEREN Infektion und im Blut sind sie die letzte und nicht die erste Bastion. Es ist - wie ich schon in meinen anderen Artikeln betonte - IMMER ein absolut feines Gleichgewicht.
Abschließend kann man also sagen: Es war eine richtig, richtig üble Idee, was Pfizer da tat. NARF.
Euer genervter Bürger.
(Vielen herzlichen Dank und noch ein extra fettes NARF an Maples für das Review und die Anregungen.)